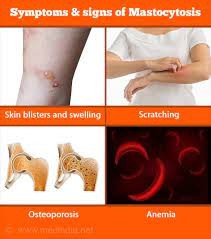
بررسی اجمالی
ماستوسیتوز اختلالی است که در آن ماست سل های غیر طبیعی در یک یا چند اندام افزایش می یابند. در این شرایط رشد ماست سل ها به خوبی کنترل نمی شود، گاهی اوقات در نتیجه جهش هایی است که کلون ها یا کپی های یکسانی از سلول ها را تولید می کنند. رشد و تکثیر ماست سل های طبیعی توسط یک پروتئین غشایی به نام KIT کنترل می شود که می تواند به عنوان یک کلید روشن و خاموش تنظیم شود. جهش در KIT که سوئیچ را روشن نگه می دارد، علت ماستوسیتوز است. رایجترین جهش به نام KIT D816V، گیرندهای تولید میکند که به طور مداوم فعال میشود و در نتیجه رشد مستمر و فعال شدن ماست سلها به وجود میآید. هنگامی که تعداد ماست سل ها افزایش می یابد، مقدار واسطه های آزاد شده افزایش می یابد و علائم مرتبط با واسطه ماست سل را ایجاد می کند که می تواند سیستمیک و در اندام های متعدد موضعی باشد.
ماست سل ها یکی از سلول های ایمنی هستند که حامل آنتی بادی آلرژیک به نام IgE هستند که به آلرژن هایی مانند گرده، بادام زمینی یا پنی سیلین متصل می شود. اتصال IgE به آلرژن ها باعث آزاد شدن واسطه های شیمیایی مانند هیستامین، تریپتاز، لکوترین ها و پروستاگلاندین ها می شود. این واسطه ها و سایر واسطه ها باعث واکنش آلرژیک می شوند. در موارد شدید میتوانند منجر به آنافیلاکسی شوند که شدیدترین واکنشهای آلرژیک است. آنافیلاکسی می تواند منجر به ایست قلبی عروقی و مرگ شود. ماست سل ها همچنین می توانند توسط سایر محرک های غیر اختصاصی مانند تغییرات دما، استرس، الکل و ورزش در میان سایر محرک ها تحریک شوند تا واسطه ها را آزاد کنند. علاوه بر افزایش واسطهها در نتیجه افزایش تعداد، ماست سلهای غیرطبیعی در ماستوسیتوز میتوانند به طور کلی مستعد انتشار آسانتر واسطهها باشند.
ماستوسیتوز بر اساس محل افزایش تعداد سلول ها، علائم و تظاهرات بالینی و یافته های پاتولوژی طبقه بندی می شود. در ماستوسیتوز جلدی، افزایش تعداد ماست سل ها فقط در پوست یافت می شود. در ماستوسیتوز سیستمیک، افزایش تعداد ماست سل ها در سایر اندام ها یافت می شود که ممکن است خوشه های ماست سل نیز در پوست وجود داشته باشند یا نه. سارکوم ماست سل یک بیماری بسیار نادر با یک توده سلول است که می تواند در هر اندامی رخ دهد. ماستوسیتوز می تواند هم در کودکان و هم در بزرگسالان رخ دهد که ماستوسیتوز پوستی در کودکان و ماستوسیتوز سیستمیک در بزرگسالان شایعتر است.
در این مقاله به ماستوسیتوز سیستمیک می پردازیم.
ماستوسیتوز سیستمیک
اکثر بزرگسالان مبتلا به ماستوسیتوز سیستمیک دارای انفیلتراسیون یک یا چند اندام داخلی با ماست سل های غیرطبیعی هستند و می توانند با یا بدون ماستوسیتوز جلدی تظاهر کنند.
علائم
در صورت وجود علائم مداوم آزادسازی واسطه ماست سل، به خصوص در غیاب محرک های شناخته شده آزادسازی واسطه ماست سل، مانند آلرژی یا برخی داروها، لازم است به ماستوسیتوز مشکوک شوید. بیماران ممکن است یک یا چند گروه از علائم ذکر شده را تجربه کنند.
علائم ماستوسیتوز عبارتند از:
محرک های بالقوه برای آزادسازی واسطه ماست سل در ماستوسیتوز عبارتند از:
تشخیص
ماستوسیتوز با نمونه برداری از بافت هایی که در آن احتمال ماست سل فراوان است با استفاده از بیوپسی، اندازه گیری واسطه های ماست سل در خون و ادرار، شمارش خون، مطالعات عملکرد کبد و آزمایش های ژنتیکی تشخیص داده می شود. اکثر بیماران بالغ مبتلا به ماستوسیتوز جلدی اندام های دیگری نیز درگیر هستند (بر خلاف مورد در اکثر کودکان). بنابراین، در بزرگسالان مهم است که به دنبال ماستوسیتوز سیستمیک احتمالی با استفاده از بیوپسی از اندام ها علاوه بر پوست باشید. نمونهبرداری از مغز استخوان معمولاً استفاده میشود، زیرا پیشسازهای ماست سل قبل از مهاجرت به سایر اندامها برای بلوغ از مغز استخوان منشأ میگیرند و در آنجا فراوانتر هستند. بیوپسی های دستگاه گوارش نیز منبع خوبی برای افزایش ماست سل ها هستند.
تشخیص ماستوسیتوز سیستمیک با معیارهای تعیین شده توسط گروه اجماع سازمان بهداشت جهانی تعیین می شود و نیاز به رعایت معیار اصلی به اضافه یک معیار جزئی یا در عوض، سه مورد از معیارهای فرعی دارد.
معیارهای اصلی: نفوذ چند کانونی متراکم ماست سل ها (MCs) (>15 MCs در مجموع) در بخش های بیوپسی رنگ آمیزی شده با تریپتاز از مغز استخوان یا سایر اندام های خارج جلدی مانند دستگاه گوارش.
معیارهای جزئی:
علاوه بر تشخیص اولیه، ماستوسیتوز سیستمیک به زیرگروه هایی تقسیم می شود که با یافته هایی مانند میزان نفوذ اندام توسط ماست سل ها (بار ماست سل ها)، وجود یا عدم وجود سایر بدخیمی های خونی و درگیری اندام ها با آسیب های مرتبط با ماست سل ها تعیین می شود از جمله بزرگ شدن کبد، طحال یا غدد لنفاوی، یا آسیب استخوان. پنج زیرگروه ماستوسیتوز سیستمیک وجود دارد و انواع نادر دیگری از جمله ماستوسیتوز سیستمیک به خوبی تمایز یافته می باشد. تعیین زیر گروه به هدایت درمان و ایجاد پیش آگهی کمک می کند. زیرگروهها در اینجا فهرست شدهاند که ماستوسیتوز سیستمیک خوش خیم شایعترین آنها است و سایر زیرگروهها به ترتیب افزایش تهاجم عبارتند از:
اکثر بیماران بالغ در دسته ماستوسیتوز سیستمیک خوش خیم قرار میگیرند اگرچه ممکن است این بیماران علائمی داشته باشند، ولی معمولاً عوارض کم و امید به زندگی طبیعی دارند که با همسالان خود تفاوتی ندارد. بیماران مبتلا به ماستوسیتوز سیستمیک فعال بقای پایین تری در مقایسه با ماستوسیتوز سیستمیک غیرفعال دارند، اما سن بالای این بیماران بیشتر تفاوت را تشکیل می دهد. بیماران مبتلا به ماستوسیتوز سیستمیک خوش خیم خطر کم پیشرفت به بیماری شدیدتر دارند، در حالی که خطر پیشرفت به بیماری شدیدتر برای بیماران ماستوسیتوز سیستمیک فعال بیشتر است.
بیماران ماستوسیتوز سیستمیک تهاجمی علائم مهم تری از جمله بزرگ شدن کبد و غدد لنفاوی و همچنین ناهنجاری های خونی مانند کم خونی و پلاکت پایین دارند. بیماران مبتلا به ماستوسیتوز سیستمیک با نئوپلاسم خونی مرتبط از مشکلات اضافی ناشی از بدخیمی خونی همراه رنج می برند. لوسمی ماست سل بسیار نادر است، اما با پیش آگهی دشوار و طول عمر کوتاه تر همراه است.
درمان
هدف از درمان کنترل اثرات واسطه های آزاد شده ماست سل با اجتناب از محرک ها و همچنین استفاده از داروهای مختلف است. بیشتر درمان ها حمایتی هستند، اما اخیراً موفقیت هایی با درمان های هدفمند وجود داشته است.
مواد موضعی مانند نرم کننده ها برای مرطوب نگه داشتن پوست و کمتر کردن تحریکات فیزیکی مهم هستند. کورتیکواستروئیدهای موضعی به طور معمول استفاده نمی شوند. آنتی هیستامین ها، از جمله آنتی هیستامین های H1 و H2، معمولاً برای جلوگیری از اثرات هیستامین سلول های ماست استفاده می شوند. تثبیت کننده های ماست سل، مانند کرومولین سدیم و کتوتیفن، همراه با عوامل بازدارنده لکوترین، ممکن است مفید باشند. ممکن است برای درمان دوره های آنافیلاکسی یا فشار خون پایین به اپی نفرین نیاز باشد. پیشنهاد می شود که بیماران مبتلا به ماستوسیتوز باید دو انژکتور اپی نفرین را به دلیل افزایش بار ماست سل و افزایش انتشار واسطه حمل کنند. اشکال تهاجمی تر ماستوسیتوز سیستمیک ممکن است به اینترفرون، تعدیل کننده های ایمنی یا عوامل شیمی درمانی نیاز داشته باشد. درمان پوکی استخوان می تواند آسیب های استخوانی را بهبود بخشد. کم خونی و تعداد کم پلاکت ها با تزریق خون درمان می شود. درمانهای هدفمند، مانند مهارکنندههای کیناز، در حال حاضر در بیماریهای تهاجمی و اخیراً برای افزایش کیفیت زندگی بیماران مبتلا به ماستوسیتوز سیستمیک خوش خیم، ارزشمند هستند.
دکتر بابک قلعه باغی
فوق تخصص آلرژی و ایمونولوژی بالینی


بررسی اجمالی
ویروس سنسیشیال تنفسی (RSV) یکی از ویروس هایی است که باعث عفونت ریه می شود. عفونت RSV می تواند در هر سنی رخ دهد و اکثر افراد سالم ظرف یک تا دو هفته بهبود می یابند. با این حال، عفونت RSV می تواند در برخی افراد، از جمله نوزادان، کودکان خردسال و بزرگسالان مسن تر، شدید باشد. کودکانی که با عفونت های RSV در دوران نوزادی خس خس می کنند، خطر ابتلا به آسم بیشتری دارند. عفونت های RSV کاملا فصلی هستند. فصل از سال به سال متفاوت است، اما عفونت ها در زمستان شایع تر هستند.
علائم و تشخیص
عفونت RSV می تواند علائمی شبیه سرماخوردگی مانند سرفه، آبریزش بینی، عطسه، تب و از دست دادن اشتها ایجاد کند. RSV می تواند باعث خس خس سینه در کودکان (برونشیولیت)، به ویژه در کودکان کمتر از 2 سال شود. در نوزادان، تنها علائم عفونت ممکن است تحریک پذیری، کاهش فعالیت و مشکلات تنفسی باشد.
برخی از کودکان به ویژه در معرض خطر ابتلا به بیماری های شدیدتر RSV هستند. اینها شامل شیرخواران مبتلا به بیماری های مزمن پزشکی (که بر ریه ها، قلب یا سیستم ایمنی بدن تأثیر می گذارد)، کودکان زیر 4 ماه و نوزادان نارس متولد شده اند.
چندین روش آزمایشگاهی مختلف برای تشخیص عفونت RSV در دسترس است.
درمان
هیچ درمان خاصی برای عفونت های RSV وجود ندارد.
کودکان مبتلا به برونشیولیت ممکن است در صورت سخت شدن تنفس نیاز به بستری شدن در بیمارستان داشته باشند. در بیشتر موارد، حتی برای کسانی که نیاز به بستری شدن در بیمارستان دارند، بهبودی معمولاً در حدود یک تا دو هفته اتفاق میافتد.
نوزادان پرخطر را می توان با آنتی بادی خنثی کننده RSV (palivizumab یا Synagis®) درمان کرد تا خطر ابتلا به بیماری های شدید RSV را کاهش دهد.
دکتر بابک قلعه باغی
فوق تخصص آلرژی و ایمونولوژی بالینی

ماست سل ها سلول های آلرژیک هستند که مسئول واکنش های آلرژیک فوری هستند. آنها با آزاد کردن محصولاتی به نام "واسطه" که در داخل آنها ذخیره شده یا ساخته شده اند، علائم آلرژیک ایجاد می کنند. در واکنشهای آلرژیک، این آزادسازی زمانی اتفاق میافتد که آنتیبادی آلرژی IgE، که در سطوح ماستسلها وجود دارد، به پروتئینهایی که آلرژیزا نامیده میشوند، متصل شود. این تحریک را فعال سازی و آزادسازی این واسطه ها را دگرانولاسیون می نامند.
برخی از این واسطهها در گرانولهایی در ماست سلها ذخیره میشوند و به سرعت آزاد میشوند و برخی دیگر تنها پس از تحریک سلول به آرامی ساخته میشوند. ماست سل ها همچنین می توانند توسط مواد دیگری مانند داروها، عفونت ها، زهر حشرات یا خزندگان فعال شوند. این پاسخ ها، اگرچه مطلوب نیستند، اما توسط ماست سل های "عادی" ایجاد می شوند. آنها را "فعال سازی ثانویه" می نامند زیرا به دلیل (ثانویه) محرک های خارجی هستند.
گاهی اوقات ماست سل ها به دلیل سیگنال های داخلی غیر طبیعی اختلال پیدا می کنند و واسطه ها را آزاد می کنند. جهشهای خاصی در ماست سلها میتوانند جمعیتهایی از ماست سلهای یکسان - به نام کلون - تولید کنند که واسطهها را بیش از حد تولید کرده و خود به خود آزاد میکنند. تولید خود به خودی واسطه ها در این اختلالات کلونال ماست سل "فعال سازی اولیه" نامیده می شود. این سلول های غیر طبیعی می توانند به طور غیرقابل کنترلی رشد کنند و به طور غیرعادی در شرایطی به نام ماستوسیتوز فعال شوند.
سندرم فعال سازی ماست سل ایدیوپاتیک
MCAS وضعیتی است که در آن بیمار دوره های مکرر علائم آنافیلاکسی را تجربه می کند - علائم آلرژیک مانند کهیر، تورم، فشار خون پایین، مشکل در تنفس و اسهال شدید. سطوح بالایی از واسطه های ماست سل در این شرایط آزاد می شوند. این دورهها به درمان با مهارکنندهها یا مسدودکنندههای واسطههای ماست سل پاسخ میدهند. این اپیزودها "ایدیوپاتیک" نامیده می شوند که به این معنی است که مکانیسم ناشناخته است - یعنی ناشی از آنتی بادی آلرژیک یا ثانویه به سایر شرایط شناخته شده ای نیست که ماست سل های طبیعی را فعال می کنند.
ارزیابی برای MCAS با تعیین اینکه آیا علائم در حملات جداگانه رخ میدهند و نشانههای معمول یک واکنش آنافیلاکتیک بدون علت واضح هستند یا خیر، شروع میشود. واسطه های ماست سل در طول دوره افزایش می یابد. این واسطهها باید در طول دورههای حاد و در ابتدا به دنبال افزایش در طول علائم اندازهگیری شوند. در نهایت، بهبود و درمان با استفاده از مهارکننده های واسطه های ماست سل تشخیص را نهایی می کند.
علائم
علائمی که بیشتر با آنافیلاکسی مطابقت دارند عبارتند از:
واسطه ها
ماست سلها مولکولهای زیادی را تولید میکنند که باعث التهاب میشوند، اما تنها تعداد کمی از واسطهها یا محصولات تجزیه پایدار آنها (متابولیتها) به طور قابل اعتمادی در حملات MCAS افزایش یافته و در روشهای آزمایشگاهی قابل اندازهگیری هستند. افزایش تریپتاز ماست سل سرم و سطوح N-methylhistamine در ادرار، 11B-Prostaglandin F2α (11B-PGF2α) و/یا Leukotriene E4 (LTE4) تنها آزمایش های مفید در تشخیص MCAS هستند.
کل تریپتاز ماست سل سرم باید بین 30 دقیقه تا دو ساعت پس از شروع یک حمله اندازه گیری شود و سطح پایه چند روز بعد اندازه گیری شود. آزمایشهای ادرار روی مجموعهای از ادرار ۲۴ ساعته انجام میشود که بلافاصله شروع میشود.
از آنجایی که این تستهای آزمایشگاهی استاندارد نیستند، بیماران باید با فوق تخصص آلرژی همکاری کنند که میتواند با پرسنل اورژانس و آزمایشگاه ارتباط برقرار کند تا از سفارش و تکمیل به موقع آنها اطمینان حاصل کند.
درمان
اهداف درمان هم تشخیص و هم تسکین بیمار است. هدف فوری ارائه تسکین برای بیمار است. عدم پاسخ به این درمان ها نشان می دهد که MCAS وجود ندارد.
درمان دورههای حاد باید از توصیههای مربوط به درمان آنافیلاکسی پیروی کند، در صورتی که علایم شدید باشد باید اپی نفرین تجویز شود.
آنتی هیستامین ها مانند بلوک کننده های گیرنده هیستامین نوع 1 نسل اول دیفن هیدرامین و هیدروکسی زین می توانند برای خارش، درد شکمی و گرگرفتگی موثر باشند، اما ممکن است مصرف آنها به دلیل عوارض جانبی (خواب آلودگی) محدود شود. آنتی هیستامین های نسل دوم از جمله لوراتادین، ستیریزین و فکسوفنادین به دلیل عوارض جانبی کمتر ترجیح داده می شوند.
درمان با مسدود کننده های گیرنده هیستامین نوع 2، مانند رانیتیدین یا فاموتیدین، می تواند برای درد شکم و حالت تهوع مفید باشد.
آسپرین تولید پروستاگلاندین D2 را مسدود می کند و می تواند گرگرفتگی را کاهش دهد.
Montelukast و zafirlukast اثرات لوکوترین C4 (LTC4) را مسدود می کنند و زیلوتون تولید LTC4 را مسدود می کند، بنابراین خس خس سینه و دل پیچه را کاهش می دهد.
کورتیکواستروئیدها
برای ادم، کهیر و خس خس سینه مفید هستند، اما فقط باید به عنوان آخرین راه حل استفاده شوند.
گزارش شده است که Omalizumab (که اتصال IgE به گیرنده های آن را مسدود می کند) واکنش پذیری ماست سل و حساسیت به فعال شدن را کاهش می دهد که می تواند دوره های آنافیلاکتیک را کاهش دهد.
خلاصه
از آنجایی که علائم آنافیلاکسی می تواند مشابه علائم ناشی از سایر بیماری هایی باشد که ماست سل ها را درگیر نمی کند، معیارهای تشخیصی تضمین می کنند که فعال شدن ماست سل مسئول این حملات است. این معیارها مستلزم وجود علائم آنافیلاکتیک، افزایش واسطههای ماست سل در طول علائم و رفع علائم با درمان مناسب است.
هنگامی که این معیارها وجود داشته باشند، آزمایشات بیشتر باید اختلالات ماست سل کلونال اولیه را که می توانند این علائم را نیز ایجاد کنند، رد کند. خون بیمار باید برای جهش کیت گیرنده رشد ماست سل به نام KIT D816V آزمایش شود. اگر مثبت باشد، نشان دهنده اختلال ماست سل کلونال است. آزمایش خون منفی برای KIT D816V مفید است اما 100٪ دقیق نیست، بنابراین باید از یکی از چندین سیستم امتیازدهی برای پیگیری علائم و نتایج آزمایشگاهی استفاده کرد تا مشخص شود که آیا بروز ژن با اختلال ماست سل کلونال مطابقت دارد یا خیر. اگر چنین است، بیوپسی مغز استخوان و آسپیراسیون اندیکاسیون دارد. بیوپسی سطح بالایی از توانایی (حساسیت) را برای یافتن جهش KIT D816V ارائه می دهد و اجازه می دهد تا ماست سل های مغز استخوان را برای شکل و نشانگرهای غیرطبیعی سطح سلول بررسی کنند. اگر بیوپسی مغز استخوان برای ماست سل های غیرطبیعی و کلونال منفی باشد، تشخیص سندرم فعال سازی ماست سل ایدیوپاتیک را مشخص می کند.
دکتر بابک قلعه باغی
فوق تخصص آلرژی و ایمونولوژی بالینی


داروهای سرکوب کننده سیستم ایمنی برای درمان بیماری های خود ایمنی
بیماری های آلرژی، ایمونولوژی و روماتولوژی اغلب به دلیل مشکلات سیستم ایمنی ایجاد می شوند. داروهای درمان بیماری های خودایمنی و آلرژیک اجزای مختلف سیستم ایمنی را هدف قرار می دهند. درمان ها ممکن است کل سیستم ایمنی یا فقط بخش های بسیار خاصی از آن را تضعیف کنند. اینکه چگونه هر یک از این داروها بخش های خاصی از سیستم ایمنی را هدف قرار می دهند ممکن است بیمار را بیشتر در معرض ابتلا به عفونت های خاص قرار دهد. در اینجا، ما در مورد طیف وسیعی از داروهای مورد استفاده برای درمان بیماری های خودایمنی، اجزای سیستم ایمنی که توسط این داروها هدف قرار می گیرند، و انواع عفونت ها (در صورت وجود) که ممکن است در افرادی که از این داروهای سرکوب کننده سیستم ایمنی مصرف می کنند، شایع تر باشند، بحث خواهیم کرد.
سیستم ایمنی دارای دو بخش است: ذاتی و اکتسابی.
سیستم ایمنی ذاتی اولین خط دفاعی در برابر باکتری ها و ویروس ها است. این دفاع ها شامل سلول ها و مولکول هایی است که در محل ورود مهاجمان خارجی (بینی، ریه ها، روده و پوست) قرار دارند. سلول های ایمنی مولکول هایی به نام سیتوکین می سازند تا بین قسمت های مختلف بدن ارتباط برقرار کنند. این سیتوکینها، مانند فاکتور نکروز تومور (TNF)، اینترلوکین-1 (IL-1) و اینترلوکین-6 (IL-6) میتوانند برای درمان بیماریهای خودایمنی مورد هدف قرار گیرند، جایی که سیستم ایمنی به سلولهای خودی بدن حمله میکند.
سیستم ایمنی اکتسابی در طول زمان توسعه می یابد. دو نوع گلبول سفید به نامهای سلولهای T و سلولهای B بخشهای مهم ایمنی اکتسابی هستند. وقتی بدن یک باکتری یا ویروس جدید می بیند، سلول های T و سلول های B می سازد که مهاجم را شناسایی کرده و به بدن کمک می کند تا از شر عفونت خلاص شود. اگر سیستم ایمنی به خوبی کار کند، پس از مبارزه با اولین عفونت، بدن آن باکتری یا ویروس را به یاد می آورد. بخشهایی از سیستم ایمنی اکتسابی نیز هدفی برای درمان بیماریهای خودایمنی هستند. ما داروهایی برای حذف سلول های B و کاهش سرعت سلول های B و سلول های T داریم. برخی از سیتوکین ها مانند اینترلوکین-17 (IL-17)، اینترلوکین-12 (IL-12) و اینترلوکین-23 (IL-23) برای ایمنی اکتسابی مهم هستند.
راه های مختلفی برای ورود این داروها به بدن شما وجود دارد. داروهای خاصی مانند استروئیدها، آزاتیوپرین و متوترکسات را می توان از طریق خوراکی مصرف کرد. داروهای دیگری که بیولوژیک نامیده می شوند، باید یا از طریق ورید به خون یا به صورت زیر جلدی در چربی زیر پوست تزریق شوند.
همچنین به خاطر داشته باشید که تحقیقات در مورد بیماری خودایمنی و درمان آن بسیار فعال است و داروها و نشانه های درمان به طور مکرر تکامل می یابند. این بحث شامل فهرست کاملی از نشانه ها یا عوارض جانبی این داروها نمی شود. برای مثال، از بارداری (چه به عنوان پدر یا مادر احتمالی) باید در بسیاری از این داروها اجتناب شود. اگر سؤال خاصی در مورد داروها یا شرایط زیر دارید، حتماً با پزشک خانواده، آلرژیست و ایمونولوژیست بالینی یا روماتولوژیست خود صحبت کنید.
سرکوبگرهای ایمنی عمومی
استروئیدها
به عنوان مثال: پردنیزون، متیل پردنیزولون، دگزامتازون
موارد مصرف: کاربردهای متعدد در بسیاری از بیماری های خودایمنی، آسم، کهیر
هدف دارویی: استروئیدها اثرات گسترده ای برای جلوگیری از التهاب دارند
نحوه کار: استروئیدها بدن را از ساخت سیتوکینهایی که باعث التهاب میشوند، متوقف میکنند، سلولهای ایمنی خاصی به نام سلولهای T و B و ائوزینوفیلها را تحلیل میبرند و حرکت سلولهای ایمنی به نقاط عفونت یا آسیب را در بدن دشوارتر میکنند. آنها با "استروئیدهای آنابولیک" که گاهی توسط ورزشکاران مورد سوء استفاده قرار می گیرند متفاوت هستند.
به چه نکاتی توجه کنید: استفاده طولانی مدت از استروئیدها شما را در معرض خطر بسیاری از مسائل مربوط به سلامت استخوان، فشار خون بالا، کنترل قند خون، آب مروارید و عفونت قرار می دهد. بسته به میزان مصرف استروئید و مدت زمانی که از آن استفاده می کنید، از نظر انواع خاصی از عفونت ها، از جمله انواع نادر پنومونی، تحت نظر خواهید بود. ممکن است برای کمک به پیشگیری از برخی انواع عفونت ها نیاز به استفاده از آنتی بیوتیک داشته باشید. اگر برای مدت کوتاهی از استروئید استفاده می کنید، معمولاً این اقدامات لازم نیست. برای کسانی که از استروئیدهای طولانی مدت استفاده می کنند، باید قبل از دریافت واکسن با پزشک خود صحبت کنند.
کلشی سین
موارد مصرف: عود نقرس، تب مدیترانه ای خانوادگی (FMF)، سایر بیماری های خود ایمنی
هدف دارویی: عملکرد نوتروفیل (نوعی گلبول سفید) را مهار می کند
نحوه عملکرد: با کاهش عملکرد نوتروفیل ها، با کاهش التهاب در بیماری های خاص عمل می کند.
به چه مواردی باید توجه کرد: کلشی سین معمولاً می تواند باعث اسهال، حالت تهوع و استفراغ شود. همچنین ممکن است باعث آسیب کبد، کلیه یا ماهیچه شود و منجر به کاهش تعداد سلول های خونی شود. این دارو ممکن است باعث تداخلات خطرناک با سایر داروها شود، بنابراین بررسی کامل داروهای مصرفی بیمار ضروری است. نباید با آب گریپ فروت مصرف شود.
هیدروکسی کلروکین (Plaquenil)
موارد مصرف: لوپوس، آرتریت روماتوئید، مالاریا، کهیر مزمن و سایر بیماری های خودایمنی
هدف دارویی: سیگنال دهی سلول های ایمنی
چگونه کار می کند: با کاهش سیگنال دهی در سیستم ایمنی، پاسخ التهابی را کاهش می دهد. ممکن است از فعال شدن برخی سلول های ایمنی به نام سلول های دندریتیک جلوگیری کند.
به چه چیزی توجه کنید: هیدروکسی کلروکی ممکن است باعث اسهال، حالت تهوع، استفراغ و درد شکم شود. همچنین ممکن است باعث ایجاد بثورات، تغییرات بینایی و کاهش سلول های خونی شود. با افزایش خطر عفونت همراه نیست. بیماران باید در حین مصرف این دارو معاینه چشمی منظم داشته باشند. تداخلات دارویی زیادی دارد.
سولفاسالازین
موارد مصرف: آرتریت روماتوئید، آرتریت روماتوئید نوجوانان، آرتریت پسوریاتیک، کولیت اولسراتیو و سایر بیماری های خود ایمنی
هدف دارویی: از تشکیل مواد شیمیایی به نام پروستاگلاندین ها جلوگیری می کند
نحوه کار: جزء فعال سولفاسالازین، 5-آمینو سالیسیلات، به کاهش تدریجی التهاب کمک می کند.
به چه مواردی باید توجه کرد: این دارو ممکن است باعث تهوع، سردرد، حساسیت به آفتاب و بثورات پوستی شود. در بیمارانی که به آنتی بیوتیک های سولفا یا سالیسیلات ها حساسیت دارند باید اجتناب شود و در بیماران مبتلا به کمبود G6PD با احتیاط مصرف شود. بیماران باید در هنگام مصرف این دارو از ضد آفتاب استفاده کنند. ممکن است به طور موقت تعداد اسپرم را کاهش دهد و باعث نارنجی شدن ادرار شود. از آنجایی که ممکن است به ندرت منجر به کاهش شمارش خون و خطر عفونت شود، ممکن است نیاز باشد در حین مصرف این دارو آزمایش خون را بررسی کنید.
داپسون
موارد مصرف: جذام و سایر عفونت ها، درماتیت هرپتی فرمیس، سایر بیماری های خود ایمنی
هدف دارویی: با سنتز فولات باکتریایی تداخل دارد
نحوه کار: همچنین از آسیب سلولی ناشی از رادیکال های آزاد جلوگیری می کند و مواد شیمیایی به نام لکوترین ها یا پروستاگلاندین ها را برای اثر ضد التهابی مهار می کند.
به چه مواردی باید توجه کرد: این دارو ممکن است باعث مشکلات دستگاه گوارش، بثورات پوستی و سردرد شود. به ندرت ممکن است باعث تغییرات خلقی، کاهش تعداد سلول های خونی، آسیب کلیه و کبد و ناباروری مردان شود. این دارو در بیماران مبتلا به کمبود G6PD باید با احتیاط مصرف شود و در بیماران مبتلا به آلرژی سولفا از مصرف آن اجتناب شود. ممکن است تداخلات دارویی زیادی داشته باشد.
متوترکسات
موارد مصرف: آرتریت روماتوئید، بسیاری از بیماری های خود ایمنی دیگر و برخی سرطان ها
هدف دارویی: نحوه استفاده سلول ها از اسید فولیک، یک ماده مغذی خاص را مسدود می کند. این بخش کلیدی در ساخت DNA و RNA است که برای رشد، تقسیم و بقای سلولهای T و سلولهای B مهم هستند.
چگونه کار می کند: سلول های T و سلول های B برای زندگی و رشد نیاز به ساخت DNA و RNA دارند. کند کردن این فرآیند به کنترل التهاب در شرایط خودایمنی کمک می کند.
به چه نکاتی توجه کنیم: متوترکسات یک داروی سرکوب کننده سیستم ایمنی است. در دوزهای پایین برای درمان بیماری های خود ایمنی استفاده می شود. هنگام مصرف متوترکسات احتمال ابتلا به عفونت های باکتریایی و ویروسی بیشتر است زیرا توانایی بدن شما برای ساخت سلول های T و B را کاهش می دهد. قبل از شروع این دارو باید از نظر عفونت های ویروسی مانند هپاتیت B و C و همچنین عملکرد کلیه و کبد خود بررسی شوید. در حین مصرف این دارو، آزمایشات کلیه و کبد شما بررسی می شود. برای کاهش عوارض جانبی این دارو مانند زخم های دهان، اسهال یا تهوع، اغلب برای بیماران اسید فولیک تجویز می شود.
مایکوفنولات موفتیل (سلسپت، مایفورتیک)
موارد مصرف: در بسیاری از بیماری های خودایمنی دیگر و پیشگیری از پس زدن در پیوند اعضای جامد استفاده می شود.
هدف دارویی: آنزیم اینوزین-5'-مونوفسفات دهیدروژناز (IMPDH)
چگونه کار می کند: آنزیم IMPDH برای ساخت DNA و RNA مهم است. سلول های T و سلول های B برای رشد و تقسیم به این آنزیم نیاز دارند و مسدود کردن آن به کنترل پاسخ های ایمنی در بیماری های خودایمنی کمک می کند.
به چه نکاتی توجه کنید: هنگام مصرف مایکوفنولات، خطر ابتلا به عفونتهای ناشی از باکتریها یا ویروسها بیشتر است، زیرا توانایی بدن شما برای ساخت سلولهای T و B را کاهش میدهد. قبل از شروع این دارو باید از نظر عفونت های ویروسی مانند هپاتیت B و C بررسی شوید. هنگام مصرف این دارو، شمارش سلول های خونی، آزمایش های کلیه و کبد شما بررسی می شود. از واکسن های زنده باید اجتناب شود.
آزاتیوپرین (ایموران)
موارد مصرف: در بسیاری از بیماری های خودایمنی دیگر و پیشگیری از رد پیوند استفاده می شود
هدف دارویی: این دارو به مولکولی تبدیل می شود که در هنگام کنار هم قرار گرفتن در DNA ساخته می شود و از ساخت صحیح DNA جلوگیری می کند. این باعث می شود سلول های T و B رشد و تقسیم آهسته تری داشته باشند.
چگونه کار می کند: سلول های T و سلول های B برای رشد و تقسیم نیاز به ساخت DNA و RNA دارند. کند کردن این روند به کنترل پاسخ های ایمنی در بیماری های خودایمنی کمک می کند.
به چه نکاتی توجه کنید: هنگام مصرف آزاتیوپرین خطر ابتلا به عفونت از باکتری یا ویروس بیشتر است زیرا توانایی بدن شما برای ساخت سلول های T و B را کاهش می دهد. قبل از شروع این دارو باید از نظر عفونت های ویروسی مانند هپاتیت B و C بررسی شوید. پزشک شما ممکن است قبل از شروع این دارو بررسی کند که آیا بدن شما پروتئینی به نام تیوپورین متیل ترانسفراز (TPMT) می سازد تا مطمئن شود بدن شما می تواند به طور معمول از اثرات آن در امان باشد یا نه. هنگام مصرف این دارو، شمارش سلول های خونی، آزمایش های کلیه و کبد شما بررسی می شود. ممکن است خطر ابتلا به بدخیمی را افزایش دهد.
ایمنی ذاتی
آنتی IL-1 بیولوژیک
مثالها: Anakinra (Kineret)، Canakinumab (Ilaris)، Rilonacept (Arcalyst)
موارد مصرف: سندرم های دوره ای مرتبط با کریوپیرین (CAPS)، از جمله سندرم خود التهابی سرد خانوادگی و سندرم ماکل ولز، آرتریت ایدیوپاتیک نوجوانان سیستمیک (کاناکینوماب)، آرتریت روماتوئید (آناکینرا)
هدف دارویی: اینترلوکین-1 (IL-1)
چگونه کار می کند: IL-1 به بدن شما کمک می کند تا هنگامی که میکروب ها با سلول ها تماس پیدا می کنند، فورا واکنش نشان دهد. این باعث تب میشود و به سلولهای دیگر میگوید به پیوستن و مبارزه با عفونت کمک کنند. با مسدود کردن IL-1، میتوانیم تب، التهاب مفاصل و پوست را کاهش دهیم و به کاهش التهاب کلی ناشی از این شرایط کمک کنیم.
به چه نکاتی توجه کنید: از آنجایی که IL-1 برای محافظت در برابر میکروب ها مهم است، با درمان طولانی مدت با آنتی IL-1 ممکن است احتمال بیشتری برای ابتلا به عفونت ها (باکتریایی و ویروسی) مانند عفونت های دستگاه تنفسی فوقانی و عفونت های دستگاه ادراری وجود داشته باشد. فعال شدن مجدد بیماری هایی مانند سل نادر است، اما انجام آزمایش عفونت سل قبل از شروع این دارو توصیه می شود. همچنین توصیه میشود که در حین مصرف این داروها از واکسنهای زنده خودداری کنید و قبل از شروع دارو، همه واکسنهای مورد نیاز از هر نوع را دریافت کنید، زیرا مشخص نیست که در زمان مصرف این نوع دارو، بدن چقدر به واکسن پاسخ میدهد. شمارش گلبول های سفید خون شما اغلب در حین مصرف این داروها کنترل می شود.
داروهای بیولوژیک ضد TNF (مهارکننده های TNF)
مثالها: اینفلیکسیماب (رمیکاد)، آدالیموماب (هومیرا)، گلیموماب (سیمپونی)، اتانرسپت (انبرل)، سرتولیزوماب (Cimzia)
موارد مصرف: آرتریت روماتوئید، پسوریازیس پلاکی/آرتریت، اسپوندیلیت آنکیلوزان، بیماری کرون، کولیت اولسراتیو
هدف دارویی: فاکتور نکروز تومور (TNF)
چگونه کار می کند: TNF برای التهابی که با تماس بدن با میکروب ها شروع می شود، مهم است. TNF التهاب را در سراسر بدن فعال می کند، باعث تب می شود و سایر گلبول های سفید خون را به قسمتی از بدن که در آن عفونت وجود دارد جذب می کند. در شرایط التهابی مانند آرتریت روماتوئید و بیماری التهابی روده، TNF می تواند باعث آسیب به مفاصل، پوست و دستگاه گوارش شود. مسدود کردن TNF می تواند به کنترل این بیماری های التهابی کمک کند.
به چه چیزی توجه کنید: TNF همچنین بخش مهمی از توانایی بدن برای خلاص شدن از شر باکتری ها، ویروس ها و قارچ های مهاجم است. هنگام مصرف درمان مسدودکننده TNF، خطر عفونت های جدی بیشتر است. علاوه بر این، شما باید از نظر سل، هپاتیت B و C، اچآیوی و غربالگری برای هرگونه خطر عفونت قارچی مورد آزمایش قرار بگیرید، زیرا اگر این عفونتها را داشته باشید، زمانی که ما TNF را مسدود کنیم، ممکن است فعال شوند. همچنین هنگام مصرف این خانواده از داروها باید از واکسن های زنده خودداری کنید. خطر طولانی مدت سرطان هایی مانند لنفوم نیز ممکن است در بیمارانی که درمان ضد TNF مصرف می کنند بیشتر باشد.
آنتی IL-6 بیولوژیک
مثال: توسیلیزوماب (Actemra)، Sarilumab (Kevzara)
موارد مصرف: آرتریت روماتوئید، آرتریت سلول غول پیکر، آرتریت ایدیوپاتیک نوجوانان
هدف دارویی: گیرنده اینترلوکین-6 (IL-6).
چگونه کار می کند: IL-6 یک سیتوکین مهم است که باعث فعال شدن سلول های T و سلول های B می شود. همچنین برای التهاب در سراسر بدن که منجر به تب می شود مهم است. در بیماری های خودایمنی مانند آرتریت روماتوئید، IL-6 باعث التهاب می شود که به مفاصل و سایر قسمت های بدن آسیب می رساند.
به چه مواردی باید توجه کرد: از آنجایی که IL-6 یک سایتوکین مهم برای بسیاری از گلبول های سفید خون و به طور کلی التهاب است، خطر عفونت با عفونت های رایج مانند ویروس های تنفسی فوقانی و عفونت های کمتر شایع مانند سل وجود دارد. . مانند درمانهای مسدودکننده TNF، قبل از شروع درمان مسدودکننده IL-6 باید از نظر سل آزمایش شوید.
سیستم کمپلمان
مثال: Eculizumab
موارد مصرف: هموگلوبینوری شبانه حمله ای (PNH)، سندرم همولیتیک اورمیک آتیپیک (a-HUS)
هدف دارویی: جزء C5 کمپلمان
چگونه کار می کند: کمپلمان بخشی از سیستم ایمنی ذاتی است که به انواع خاصی از باکتری ها (مانند نایسریا - خانواده باکتری هایی که باعث سوزاک و مننژیت مننگوکوکی می شوند) متصل می شود و آنها را از بین می برد. در شرایط عادی، بدن با داشتن پروتئین برای جلوگیری از فعال شدن کمپلمان، عملکرد نابجای آن را کنترل می کند. در شرایط خاصی مانند PNH و a-HUS، بدن نمی تواند از فعال شدن کمپلکان جلوگیری کند و بدن سلول های خود را از بین می برد. Eculizumab به جلوگیری از این نوع فعال سازی خود به خودی کمپلمان کمک می کند.
به چه مواردی باید توجه کرد: از آنجایی که کمپلمان برای دفاع بدن در برابر نایسریا بسیار مهم است، افرادی که اکولیزوماب مصرف می کنند بیشتر به این عفونت مبتلا می شوند. قبل از شروع این دارو باید علیه مننگوکوک واکسینه شده و در حین مصرف این دارو برای جلوگیری از عفونت آنتی بیوتیک مصرف کنید.
ایمنی اکتسابی - سلول های B
ضد CD20 بیولوژیک
مثال: ریتوکسیماب (Rituxan)
موارد مصرف: لنفوم غیر هوچکین، لوسمی لنفوسیتی مزمن، آرتریت روماتوئید، واسکولیت (مانند گرانولوماتوز همراه با پلی آنژیت و پلی آنژیت میکروسکوپی)، بیماری پوستی خود ایمنی
هدف دارویی: CD20، یک پروتئین سطحی روی سلول های B است
چگونه کار می کند: ریتوکسیماب به پروتئین CD20 روی سلول های B متصل می شود و سلول های B را در جریان خون از بین می برد. بیماریهایی که با ریتوکسیماب درمان میشوند، همگی به رشد سلولهای B نیاز دارند (مانند لنفوم) یا آنتیبادیهایی می سازند که به قسمتهای خاصی از بدن ما متصل میشوند و باعث التهاب میشوند (مانند آرتریت روماتوئید، واسکولیت، و بیماری پوستی خود ایمنی). وقتی سلولهای B توسط ریتوکسیماب حذف میشوند، بدن از مشکلات ناشی از سلولهای B در حال رشد و سلولهای B که آنتیبادیهای ایجادکننده بیماری را میسازند، خلاص میشود.
به چه مواردی باید توجه کرد: وقتی سلول های B از بدن خارج می شوند، خطر بیماری هایی که به طور معمول توسط آنتی بادی ها پاک می شوند، بیشتر می شود. این شامل عفونت در سینوس ها و ریه ها است. بیماریهای خاصی مانند هپاتیت B میتوانند پس از ریتوکسیماب دوباره فعال شوند و قبل از درمان باید از نظر هپاتیت B آزمایش شوید. انواع دیگری از عفونت های ویروسی مانند تبخال نیز دیده شده است. پاسخ به واکسن ها نیز پس از ریتوکسیماب محدود است و همه واکسن های مورد نیاز باید قبل از استفاده از آن تزریق شوند. در اکثر افرادی که ریتوکسیماب دریافت می کنند، سلول های B در عرض یک سال به حد طبیعی برمی گردند. با این حال، در زیرمجموعهای از افرادی که با ریتوکسیماب درمان میشوند، سلولهای B به حد طبیعی برنمیگردند و ممکن است سطوح آنتیبادی پایینی برای سالها یا مادامالعمر داشته باشید. این می تواند شما را در معرض خطر بیشتری برای عفونت قرار دهد.
بیولوژیک های ضد فاکتور رشد سلولی B
مثالها: بلیموماب (Benlysta)
موارد مصرف: لوپوس اریتماتوز سیستمیک
هدف دارویی: BLyS (محرک لنفوسیت B که BAFF نیز نامیده می شود)
چگونه کار می کند: بلیموماب سیتوکین BLyS را هدف قرار می دهد که پروتئین مهمی برای بقا و رشد سلول های B است. با مسدود کردن این فاکتور رشد در بیماران مبتلا به لوپوس، میتوانید برخی از آنتیبادیهای خودایمنی که توسط سلولهای B ساخته میشوند را کاهش دهید.
به چه نکاتی توجه کنیم: در بیمارانی که بلیموماب استفاده می کنند، عفونت های پوستی و ذات الریه شایع ترین عفونت ها هستند. بیمارانی که بلیموماب مصرف می کنند و عملکرد ایمنی آنها کاهش می یابد نیز احتمال بیشتری دارد که به ذات الریه ناشی از قارچ یا سیتومگالوویروس مبتلا شوند. هنگام مصرف بلیموماب باید از واکسن های زنده خودداری کرد.
ایمنی اکتسابی - سلول های T
مثال: سیکلوسپورین
موارد مصرف: جلوگیری از رد پیوند عضو، بیماری پیوند در مقابل میزبان، آرتریت روماتوئید، پسوریازیس، کهیر مزمن
هدف دارویی: کلسینورین، که سیگنال هایی برای فعال کردن سلول های T می دهد
چگونه کار می کند: سیکلوسپورین یک داروی خوراکی است که در سلول های T جذب می شود و در آنجا به پروتئینی به نام کلسینورین متصل می شود. وقتی این اتفاق می افتد، سلول های T نمی توانند سیتوکین بسازند یا سلول های T بیشتری بسازند.
به چه مواردی باید توجه داشت: شایع ترین عوارض جانبی سیکلوسپورین فشار خون بالا و کاهش عملکرد کلیه است و این موارد نیاز به نظارت دقیق دارند. از آنجایی که سیکلوسپورین سلول های T را مسدود می کند، یک داروی سرکوب کننده سیستم ایمنی است. ممکن است خطر بدخیمی را افزایش دهد. به طور کلی در هنگام مصرف این دارو در معرض خطر بیشتری برای ابتلا به عفونت هستید. به همین دلیل، توصیه میشود هنگام مصرف این دارو از تمام واکسنهای زنده خودداری کنید.
T Cell Co-stimulation and Activation
(تحریک وفعال کردن همزمان سلول های T)
مثال: آباتاسپت (اورنسیا)
موارد مصرف: آرتریت روماتوئید، آرتریت ایدیوپاتیک نوجوانان، آرتریت پسوریاتیک
هدف دارویی: CTLA-4/CD28
چگونه کار می کند: سلول های T توسط دو سیگنال فعال می شوند. اولین سیگنال زمانی است که گیرنده سلول T به بخش خاصی از یک میکروب (آنتی ژن) که توسط یک سلول ایمنی به نام سلول ارائه دهنده آنتی ژن (APC) به آن آورده شده است، متصل می شود. سیگنال دوم زمانی رخ می دهد که سلول T و APC توسط مجموعه دوم پروتئین در هنگام تعامل این سلول ها با هم ارتباط برقرار می کنند. نمونه ای از این سیگنال دوم یک پروتئین سلول T به نام CD28 است که به پروتئین های APC CD80/86 متصل می شود و سلول های T و APC را فعال می کند. برای خاموش کردن خود، سلول T CTLA-4 را وارد می کند که اتصال CD28 به CD80/86 را مسدود می کند. آباتاسپت فرم دارویی CTLA-4 است. با استفاده از این دارو، ما قادریم پاسخ ایمنی سلول T را خاموش کنیم. در آرتریت التهابی، این به آرام کردن التهاب ناشی از سلول های T که باعث درد و تورم مفاصل می شود، کمک می کند.
به چه نکاتی توجه کنید: از آنجایی که آباتاسپت به خاموش کردن تمام پاسخ های سلول های T کمک می کند، هنگام مصرف این دارو در معرض خطر بیشتری برای ابتلا به عفونت هستید. شما باید برای سل و هپاتیت B و C آزمایش شوید زیرا اگر این عفونت ها را داشته باشید، زمانی که فعالیت سلول های T را کم کنیم، می توانند فعال شوند. واکسن های زنده نباید به طور همزمان یا ظرف 3 ماه پس از قطع این دارو تزریق شوند.
ایمنی اکتسابی - سیتوکین ها
آنتی IL-17 بیولوژیک
مثالها: سکوکینوماب (کوسنتیکس)، ایکسیکیزوماب (تالتز)، برودالوماب (سیلیک)
موارد مصرف: پسوریازیس، آرتریت پسوریاتیک، اسپوندیلیت آنکیلوزان
هدف دارویی: IL-17 (secukinumab، ixekizumab) و گیرنده IL-17 (brodalumab)
چگونه کار می کند: IL-17 یک سایتوکین مهم در بیماری خود ایمنی است. در بیماری هایی مانند پسوریازیس و اسپوندیلیت آنکیلوزان مهم است. به طور معمول، IL-17 بخش مهمی از دفاع ما در برابر عفونت های باکتریایی و قارچی با به کارگیری انواع دیگر گلبول های سفید خون به نام نوتروفیل ها در محل های عفونت است.
به چه مواردی باید توجه کرد: هنگامی که داروهای مهار کننده IL-17 مصرف می شود، احتمال بیشتری برای عفونت وجود دارد، عمدتاً از جمله عفونت های دستگاه تنفسی فوقانی. عفونت های جدی و عفونت های قارچی در مطالعات این نوع داروها نادر بود. هنگام استفاده از درمان مسدودکننده IL-17 باید از واکسن های زنده اجتناب شود.
آنتی IL-23 بیولوژیک
مثال: گوسل کوماب (ترمفیا)
موارد مصرف: پسوریازیس
هدف دارویی: سیتوکین IL-23
چگونه کار می کند: IL-23 یک سیتوکین برای زنده نگه داشتن نوعی از سلول T به نام سلول های Th17 (که IL-17 را می سازد) مهم است. با زنده و فعال نگه داشتن این سلول ها، IL-23 بخش مهمی از دفاع بدن در برابر عفونت باکتریایی و سایر عفونت های روده است. در بیماری های خودایمنی مانند پسوریازیس، IL-23 می تواند بخشی از پاسخ التهابی باشد که باعث التهاب و علائم پوست می شود.
به چه مواردی باید توجه کرد: مسدود کردن IL-23 تأثیر زیادی بر تعداد عفونتهایی که بیماران در طول آزمایشهای بالینی داشتند، ندارد.
Anti-IL-12/23 Biologics
مثال: Ustekinumab (Stelara)
موارد مصرف: پسوریازیس، آرتریت پسوریاتیک، بیماری کرون
هدف دارویی: گیرنده های سیتوکین IL-12 و IL-23
چگونه کار می کند: Ustekinumab به بخشی از گیرنده های IL-12 و IL-23 که IL-12p40 نامیده می شود، متصل می شود. IL-12 یک سایتوکین مهم برای فعال کردن سلول های T و سایر گلبول های سفید خون به نام سلول های کشنده طبیعی است که به پاکسازی عفونت های باکتریایی و ویروسی کمک می کند. هنگامی که این سیتوکین ها به طور غیر طبیعی در بیماری خودایمنی افزایش یابند، می تواند باعث آسیب به بافت ها شود، همانطور که در پسوریازیس و بیماری کرون دیده می شود.
به چه مواردی باید توجه کرد: از آنجایی که IL-12 بخش مهمی از سیستم ایمنی برای فعال کردن سلول های T است، ممکن است بیماران را در معرض خطر بالاتر عفونت ناشی از مایکوباکتریوم، سالمونلا، و سل یا BCG قرار دهد. به نظر می رسد این بسیار نادر است. قبل از شروع درمان با استکینوماب، آزمایش سل توصیه می شود.
آنتی IL-5 بیولوژیک
مثالها: Mepolizumab (Nucala)، Reslizumab (Cinqair)، Benralizumab (Fasenra)
موارد مصرف: آسم شدید ائوزینوفیلیک، سایر اختلالات مرتبط با ائوزینوفیلیک، رینوسینوزیت مزمن همراه با پولیپ بینی
هدف دارویی: IL-5 (mepolizumab و reslizumab)، گیرنده IL-5 (benralizumab)
چگونه کار می کند: IL-5 یک سیتوکین مهم برای نوع خاصی از گلبول های سفید خون به نام ائوزینوفیل است. ائوزینوفیلها برای بدن در مبارزه با عفونتهای انگلی کرمی مهم هستند و در شرایط آلرژیک مانند آسم فعال میشوند.
به چه نکاتی توجه کنید: اگر عفونت کرمی دارید، باید قبل از شروع این داروها آن را درمان کنید. اگر در حین مصرف داروهای ضد IL-5 دچار عفونت کرمی شدید که با درمان برطرف نشد، باید این داروها را قطع کنید.
آنتی IL-4/IL-13 بیولوژیک
مثال: دوپیلوماب (دوپیکسنت)
موارد مصرف: درماتیت آتوپیک، آسم، رینوسینوزیت مزمن همراه با پولیپ بینی
هدف دارویی: گیرنده آلفا IL-4 (بخشی از گیرنده IL-4 و IL-13)
چگونه کار می کند: سیتوکین های IL-4 و IL-13 در پاسخ ایمنی که منجر به تولید آنتی بادی های آلرژیک (IgE)، مخاط در راه های هوایی و فعال شدن پاسخ ایمنی آلرژیک می شود، نقش دارند.
به چه مواردی باید توجه کرد: توصیهها این است که از واکسنهای زنده (مانند MMR و واریسلا) در هنگام استفاده از دوپیلوماب اجتناب کنید. پاسخ به واکسن های کشته یا غیرفعال (مانند واکسن مننژیت) هنگام استفاده از این دارو طبیعی است. به احتمال زیاد خطر ابتلا به عفونت های پوستی، آنفولانزا یا عفونت های ویروسی سرماخوردگی وجود ندارد یا افزایش بسیار کمی دارد. IL-4 و IL-13 احتمالاً در کنترل عفونتهای کرمی مهم هستند. مطالعات تأثیر دوپیلوماب را بر این نوع عفونت ها اندازه گیری نکرده اند. اگر در منطقهای زندگی میکنید که انگلهای کرمی وجود دارد، باید بهطور دورهای تحت نظر قرار بگیرید یا در صورت داشتن علائم، مورد آزمایش قرار بگیرید.
داروی بیولوژیکی که IgE را هدف قرار می دهد
مثالها: Omalizumab (Xolair)
موارد مصرف: آسم آلرژیک، کهیر مزمن، رینوسینوزیت مزمن همراه با پولیپ بینی
هدف دارویی: IgE – آنتی بادی آلرژی
چگونه کار می کند: IgE اغلب به عنوان "آنتی بادی آلرژی" نامیده می شود. هنگامی که IgE به یک آلرژن متصل می شود، باعث آزاد شدن هیستامین و سایر مولکول هایی می شود که باعث واکنش آلرژیک (خارش، قرمزی، کهیر) می شوند.
به چه مواردی باید توجه کرد: مسدود کردن IgE تأثیر زیادی بر توانایی بدن در مبارزه با عفونتهای باکتریایی و ویروسی معمولی ندارد. IgE ممکن است برای حمله به سایر انواع عفونتها مانند انگل های کرمی (مانند کرم گرد، کرم قلابدار، کرم شلاقی، کرم نخی) مهم باشد. مطالعات نشان داده اند که در صورت استفاده از omalizumab، خطر ابتلا به عفونت در مناطقی از جهان که این انگل ها در آن زندگی می کنند افزایش می یابد. اگر در منطقهای زندگی میکنید که انگلهای کرمی وجود دارد، باید بهطور دورهای تحت نظر قرار بگیرید یا در صورت داشتن علائم، مورد آزمایش قرار بگیرید.
داروهای مهارکننده حرکت لنفوسیت ها (گلبول های سفید).
مثالها: ودولیزوماب (Entyvio)
موارد مصرف: بیماری التهابی روده (کولیت اولسراتیو و کرون)
هدف دارویی: اینتگرین α4β7 (پروتئینی در قسمت بیرونی گلبول های سفید خون که به آنها کمک می کند تا به روده برسند)
چگونه کار می کند: گلبول های سفید خون با اینتگرین α4β7 به روده می روند و در آنجا می توانند اثرات التهابی در بیماری التهابی روده داشته باشند. ودولیزوماب رفتن این سلول ها به روده را مسدود می کند و سبب کاهش میزان التهاب می شود.
به چه مواردی باید توجه کرد: میزان عفونت کلی (از جمله عفونت های سینوسی و عفونت های ادراری) در بیمارانی که از vedolizumab استفاده می کنند کمی بالاتر است. برای عفونتهای روده، گزارشهایی مبنی بر وجود آبسه در قسمت تحتانی دستگاه گوارش و عفونتهای باکتریایی در بیمارانی که از این دارو استفاده میکنند، وجود دارد.
داروهای ضد مولکول های کوچک
مهارکننده های JAK
مثال: توفاسیتینیب (Xeljanz)، آپاداسیتینیب (Rinvoq)، باریسیتینیب (Olumiant)
موارد مصرف: آرتریت روماتوئید، آرتریت پسوریاتیک، کولیت اولسراتیو
هدف دارویی: آنزیم JAK (Janus Kinase).
چگونه کار می کند: آنزیم های JAK پروتئین های مهمی در داخل سلول ها هستند که سیگنال ها را از بیرون سلول به هسته یا ماشین آلات داخل سلول منتقل می کنند. بسیاری از سیگنال های سیتوکین مختلف از JAK برای انتقال پیام در سلول ها استفاده می کنند. در بیماری هایی که التهاب بیش از حد وجود دارد، مسدود کردن JAKs می تواند (با کاهش سیگنال هایی که به سلول می گوید مولکول های التهابی مانند سیتوکین ها را بسازد و آزاد کند)، به کاهش میزان التهاب کمک می کند.
به چه مواردی باید توجه کرد: مانند سایر داروهای سرکوب کننده سیستم ایمنی، میزان عفونت با مهارکننده های JAK افزایش می یابد. یکی از ویروس هایی که بیشتر در بیمارانی که از مهارکننده های JAK استفاده می کنند، یافت شده است، هرپس زوستر است. واکسن های زنده نباید به طور همزمان تزریق شوند.
دکتر بابک قلعه باغی
فوق تخصص آلرژی و ایمونولوژی بالینی

بررسی اجمالی
سندرم هیپرئوزینوفیلیک (hy-per-ee-o-sin-o-FILL-ick) (HES) گروهی از اختلالات خونی نادر است. زمانی اتفاق می افتد که خون فرد دارای تعداد بسیار بالایی ائوزینوفیل باشد. ائوزینوفیل نوعی گلبول سفید است که نقش مهمی در سیستم ایمنی دارد.
اکثر افراد کمتر از 500 ائوزینوفیل در میکرولیتر در خون خود دارند. افراد مبتلا به HES معمولاً بیش از 1500 ائوزینوفیل در میکرولیتر به مدت 6 ماه یا بیشتر در خون خود دارند و علت آن قابل شناسایی نیست.
این ائوزینوفیل ها به بافت های مختلف راه پیدا می کنند و باعث التهاب و در نهایت اختلال در عملکرد اندام می شوند. شایع ترین اندام های درگیر در HES شامل پوست، ریه ها، قلب و سیستم عصبی است.
علائم و تشخیص
علائم
HES در هر سنی ممکن است رخ دهد، اگرچه در بزرگسالان شایع تر است. افراد مبتلا به HES ممکن است از طیف گسترده ای از علائم رنج ببرند، بسته به اینکه کدام قسمت از بدن تحت تاثیر قرار گرفته است. این علائم عبارتند از:
بثورات پوستی مانند کهیر یا آنژیوادم
سرگیجه
از دست دادن حافظه یا سردرگمی
سرفه کردن
تنگی نفس
خستگی
تب
زخم های دهان
تشخیص
علائم HES در بسیاری از مشکلات پزشکی دیگر نیز رایج است و تشخیص اولیه را دشوارتر می کند. اولین قدم این است که سایر شرایط با علائم مشابه را رد کنید. این موارد عبارتند از عفونت انگلی، بیماری آلرژیک، سرطان، بیماری های خودایمنی و واکنش های دارویی.
فوق تخصص آلرژی و ایمونولوژی بالینی آموزش تخصصی برای تشخیص موثر مشکل و همکاری با سایر متخصصان مانند هماتولوژیست یا متخصص قلب در درمان و نظارت بر HES دارد.
آزمایش بر اساس علائم فردی است و ممکن است شامل ارزیابی مدفوع برای تشخیص عفونت انگلی، آزمایش آلرژی برای تشخیص آلرژی های محیطی یا غذایی، بیوپسی از پوست یا سایر اندام ها، آزمایش خون برای غربالگری خودایمنی یا تصویربرداری CT از اندام های آسیب دیده، و مطالعات ژنتیکی مولکولی باشد. تشخیص ژن FIP1L1-PDGFRA یا سایر جهشها برای کمک به تعیین، تشخیص، پیش آگهی و درمان کمک کننده است.
هنگام تشخیص HES، تعیین میزان آسیب اندام مهم است. رادیوگرافی قفسه سینه و اکوکاردیوگرافی به طور معمول برای ارزیابی قلب و ریه ها انجام می شود. سایر آزمایشات که اغلب در بیماران HES انجام می شود شامل عملکرد کبد و کلیه، سطح ویتامین B12 سرم، میزان رسوب گلبول قرمز (ESR) و سطح تریپتاز سرم است.
درمان
هدف از درمان HES کاهش سطح ائوزینوفیل در خون و بافتها و در نتیجه جلوگیری از آسیب بافتی بهویژه در قلب است. درمان استاندارد HES شامل داروهای گلوکوکورتیکواستروئیدی مانند پردنیزون و عوامل شیمی درمانی مانند هیدروکسی اوره، کلرامبوسیل و وین کریستین است. اینترفرون آلفا نیز ممکن است به عنوان یک درمان استفاده شود. این دارو باید با تزریق مکرر تجویز شود.
تحقیقات در حال کشف درمان های جدید برای HES است. یک رویکرد جدید برای کنترل رشد سلول های بدخیم استفاده از مهارکننده های تیروزین کیناز مانند GleevecTM (imatinib) است. درمان آنتی بادی مونوکلونال، مانند آلمتوزوماب (ضد CD52) نیز برای درمان HES امیدوار کننده است. در واقع، بر اساس یک کارآزمایی تصادفیشده و کنترلشده با پلاسبو، فاز III اخیر، آنتیبادی مونوکلونکال Nucala یا mepolizumab (ضد IL-5) به تازگی توسط سازمان غذا و داروی ایالات متحده برای درمان بزرگسالان و کودکان بیش از 12 سال (مبتلا به HES به مدت شش ماه یا بیشتر بدون علت قابل شناسایی غیر مرتبط با بیماری) تایید شده است.
پیش آگهی HES به میزان آسیب هر عضو بستگی دارد. در موارد بسیار شدید، HES ممکن است کشنده باشد، اما در سالهای اخیر میزان بقا بسیار بهبود یافته است. در سال 1975، تنها 12 درصد از بیماران HES سه سال زنده ماندند. امروزه بیش از 80 درصد بیماران HES پنج سال یا بیشتر زنده می مانند.
دکتر بابک قلعه باغی
فوق تخصص آلرژی و ایمونولوژی بالینی

بررسی اجمالی
مسمومیت هیستامین که به عنوان مسمومیت اسکمبروئید نیز شناخته می شود، نوعی مسمومیت غذایی است.
گاهی اوقات مسمومیت هیستامین با واکنش آلرژیک به ماهی اشتباه گرفته می شود. زیرا:
برخی از انواع ماهی ها به طور طبیعی حاوی مقادیر بالایی از ماده شیمیایی هیستیدین هستند. این ماده شیمیایی می تواند توسط باکتری ها به هیستامین تبدیل شود. در یک واکنش آلرژیک، ماست سل ها هیستامین آزاد می کنند که باعث ایجاد علائم آلرژی می شود. بنابراین، اگر فردی ماهی بخورد که سطح هیستامین بالایی دارد، واکنش ممکن است شبیه واکنش آلرژیک به آن غذا باشد.
انواع خاصی از ماهی ها بیشتر مستعد ایجاد مسمومیت هیستامین هستند. اینها عبارتند از ماهی تن، ماهی خال مخالی، ماهی ماهی، ماهی کولی، شاه ماهی، ماهی آبی، کهربا و مارلین.
شایع ترین علت مسمومیت حاد هیستامین، نتیجه نگهداری ناکافی در یخچال یا فاسد شدن ماهی است. این باعث رشد بیش از حد باکتری می شود که هیستیدین را به سطوح بالای هیستامین تبدیل می کند.
افرادی که سطح آنزیم دی آمین اکسیداز به طور غیرمعمول پایینی دارند ممکن است بیشتر مستعد مسمومیت هیستامین باشند.
علائم و تشخیص
علائم مسمومیت هیستامین (مسمومیت اسکومبروئید) معمولاً در عرض 5 تا 30 دقیقه پس از خوردن ماهی فاسد شروع می شود، اگرچه مواردی وجود دارد که علائم تا دو ساعت به تعویق می افتد.
این علائم ممکن است شامل موارد زیر باشد:
علائم معمولاً چند ساعت یا یک روز طول می کشد. در موارد نادر، علائم ممکن است برای چند روز باقی بماند.
تشخیص این بیماری اغلب بر اساس شرایط بالینی است. به عنوان مثال، شیوع علائم معمولی که چندین نفر را تحت تاثیر قرار می دهد که یک محصول آلوده را خورده اند به احتمال زیاد نشان دهنده مسمومیت هیستامین است.
در موارد فردی، اگر فردی علائم شدیدی را تجربه کرد، بهتر است برای تعیین اینکه آیا آلرژی غذایی وجود دارد یا خیر، با فوق تخصص آلرژی و ایمونولوژی بالینی مشورت کند.
درمان
درمان مسمومیت هیستامین به شدت علائم بستگی دارد. در موارد خفیف، علائم در مدت کوتاهی بدون دارو از بین می روند. گاهی اوقات آنتی هیستامین ها می توانند کمک کننده باشند.
در موارد شدید، مراجعه به اورژانس بیمارستان برای دریافت مایعات وریدی، اکسیژن یا سایر داروها و درمانها ضروری است.
دکتر بابک قلعه باغی
فوق تخصص آلرژی و ایمونولوژی بالینی


بررسی اجمالی
بیماری ریفلاکس معده (GERD) یک اختلال گوارشی است که زمانی رخ می دهد که محتویات اسیدی معده، یا غذا و مایعات از معده به مری برگردد. افراد در تمام سنین را تحت تاثیر قرار می دهد - از نوزادان تا بزرگسالان مسن تر.
افراد مبتلا به آسم بیشتر در معرض خطر ابتلا به GERD هستند. شعله ور شدن آسم می تواند باعث شل شدن اسفنکتر تحتانی مری شود و به محتویات معده اجازه می دهد تا به مری برگردد یا رفلاکس کند. برخی از داروهای آسم (به ویژه تئوفیلین) ممکن است علائم ریفلاکس را بدتر کنند.
از سوی دیگر، ریفلاکس اسید می تواند علائم آسم را با تحریک راه های هوایی و ریه ها بدتر کند. این به نوبه خود می تواند منجر به آسم به تدریج جدی تر شود. همچنین، این تحریک می تواند واکنش های آلرژیک ایجاد کند و راه های هوایی را نسبت به شرایط محیطی مانند دود یا هوای سرد حساس تر کند.
علائم و تشخیص
علائم
همه افراد رفلاکس معده به مری را تجربه کرده اند. زمانی اتفاق می افتد که آروغ می زنید، طعم اسید در دهان دارید یا سوزش سر دل دارید. با این حال، اگر این علائم با زندگی روزمره شما تداخل داشته باشد، وقت آن است که به پزشک خود مراجعه کنید.
علائم دیگری که کمتر اتفاق میافتند، اما میتوانند نشان دهنده ابتلا به GERD باشند عبارتند از:
تشخیص
چندین آزمایش ممکن است برای تشخیص GERD استفاده شود از جمله:
درمان
اگر هم مبتلا به GERD و هم آسم هستید، درمان GERD به کنترل علائم آسم شما کمک می کند.
مطالعات نشان داده است که افراد مبتلا به آسم و GERD پس از درمان بیماری ریفلاکس، علائم آسم (و مصرف داروهای آسم) را کاهش دادند.
تغییرات سبک زندگی برای درمان GERD عبارتند از:
پزشک شما همچنین ممکن است داروهایی را برای درمان رفلاکس یا تسکین علائم توصیه کند. آنتی اسیدهای بدون نسخه و مسدود کننده های H2 ممکن است به کاهش اثرات اسید معده کمک کنند. مهارکننده های پمپ پروتون تولید اسید را مسدود می کنند و ممکن است موثر باشند.
در موارد شدید و عدم تحمل دارو، ممکن است جراحی توصیه شود.
دکتر بابک قلعه باغی
فوق تخصص آلرژی و ایمونولوژی بالینی

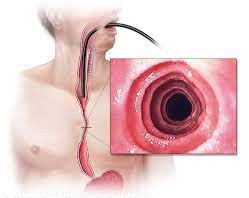
ازوفاژیت ائوزینوفیلیک (e-o-sin-o-FILL-ik) (EoE) یک بیماری مزمن آلرژیک مری است. مری لوله ای است که غذا را از دهان به معده می فرستد. در EoE، تعداد زیادی گلبول سفید به نام ائوزینوفیل در پوشش داخلی مری یافت می شود. ائوزینوفیل ها می توانند موادی را در بافت های اطراف آزاد کنند که باعث التهاب می شود. به طور معمول هیچ ائوزینوفیل در مری وجود ندارد. فرد مبتلا به EoE دارای التهاب و افزایش تعداد ائوزینوفیل ها در مری خواهد بود. التهاب مزمن EoE منجر به علائم می شود.
علائم EoE با سن متفاوت است. نوزادان و کودکان نوپا ممکن است از خوردن امتناع کنند یا به درستی رشد نکنند. کودکان در سنین مدرسه اغلب کاهش اشتها، دردهای مکرر شکم و مشکل در بلع یا استفراغ دارند. نوجوانان و بزرگسالان ممکن است علائم مشابهی داشته باشند، اما اغلب در بلعیدن غذاهای خشک یا متراکم و جامد مشکل دارند. مشکل بلع به این دلیل است که مری ملتهب است و در موارد شدید به این دلیل که مری به حد زیادی باریک می شود که غذا گیر می کند. غذایی که محکم در مری گیر کرده است، اگر از مری به داخل معده نرود یا به سرعت استفراغ نشود، می تواند یک اورژانس پزشکی باشد.
متخصصان آلرژی و گوارش بیماران بسیاری را با EoE می بینند. این به دلیل افزایش بروز EoE و آگاهی بیشتر پزشکان است. EoE به عنوان یک بیماری مزمن در نظر گرفته می شود که می توان آن را از نظر پزشکی مدیریت کرد، اما بطور کامل برطرف نمی شود.
ائوزینوفیل ها را می توان در بافت مری در بیماری هایی غیر از EoE یافت. یک مثال رایج بیماری رفلاکس اسید است. سایر بیماریهایی که میتوانند باعث وجود ائوزینوفیلها در مری شوند، قبل از تشخیص دقیق EoE باید رد شوند.
تشخیص ازوفاژیت ائوزینوفیلیک
در حال حاضر انجام آندوسکوپی فوقانی همراه با بیوپسی از مری برای تشخیص EoE ضروری است. آندوسکوپی یک روش پزشکی است که در آن یک لوله منعطف حاوی منبع نور و یک لنز دوربین از مری عبور میکند تا پزشک شما ببیند که آیا مری شما ملتهب است یا خیر. قطعات کوچکی از بافت مری به اندازه نوک قلم (بیوپسی) گرفته می شود تا از نظر وجود ائوزینوفیل ها و علائم التهاب زیر میکروسکوپ بررسی شود.
معیارهای خاصی برای تشخیص EoE وجود دارد که توسط متخصصین آلرژی، گوارش و پاتولوژیست رعایت می شود. اینها شامل علائم سازگار با EoE در ترکیب با یافته های آندوسکوپی فوقانی و پس از بررسی بیوپسی بافت مری توسط پاتولوژیست است که EoE را تایید می کند.
ازوفاژیت ائوزینوفیلیک و آلرژی
اکثر بیماران مبتلا به EoE آتوپیک هستند. فرد آتوپیک کسی است که علائم یک یا چند اختلال آلرژیک را دارد. اینها عبارتند از آسم، رینیت آلرژیک، درماتیت آتوپیک (اگزما) و آلرژی غذایی. EoE گاهی اوقات در سایر اعضای خانواده رخ می دهد. از آنجایی که بسیاری از بیماران مبتلا به EoE آتوپیک هستند، ممکن است ابتدا توسط یک متخصص آلرژی که به تشخیص مشکوک است بیمار را ببیند و برای تایید EoE به متخصص گوارش ارجاع دهد. از طرف دیگر، اگر تشخیص EoE توسط متخصص گوارش انجام شود، ممکن است برای آزمایش آلرژی به یک متخصص آلرژی ارجاع داده شوید. این اطلاعات به شما، خانواده شما و متخصص گوارش ارائه می دهد تا هر گونه جنبه آلرژیک EoE به درستی درمان شود. همچنین ممکن است به برنامه ریزی رژیم درمانی و در نهایت وارد کردن مجدد غذاها به رژیم غذایی شما کمک کند.
ازوفاژیت ائوزینوفیلیک: آلرژی های محیطی
آلرژی های محیطی به موادی مانند گرده ها، حیوانات، مایت های گرد و غبار و کپک ها احتمالاً در EoE نقش دارند. برای برخی از بیماران، ممکن است به نظر برسد که EoE آنها در فصول گرده افشانی بدتر است. آزمایش آلرژی برای این آلرژی های رایج محیطی اغلب بخشی از ارزیابی EoE است.
ازوفاژیت ائوزینوفیلیک: آلرژی غذایی
پاسخ های ایمنی نامطلوب به غذا علت اصلی EoE در تعداد زیادی از بیماران است. متخصصان آلرژی در ارزیابی و درمان EoE مرتبط با آلرژی غذایی متخصص هستند. با این حال، رابطه بین آلرژی غذایی و EoE پیچیده است. در آلرژی غذایی کلاسیک با واسطه ایمونوگلوبولین E (IgE)، محرک ها به راحتی با سابقه یک واکنش آلرژیک شدید مانند کهیر و استفراغ در عرض چند دقیقه پس از مصرف غذای مزاحم تشخیص داده می شوند. در EoE، تعیین نقش غذاها دشوارتر است، زیرا واکنشها به تأخیر میافتند و میتوانند در طول روز ایجاد شوند و تعیین دقیق یک غذای خاص به عنوان محرک را دشوارتر میکند. متخصصان آلرژی ممکن است تست های آلرژی مختلفی را برای شناسایی حساسیت به غذاهایی که ممکن است در ایجاد EoE نقش داشته باشند، انجام دهند. غذاهایی مانند محصولات لبنی، تخم مرغ، سویا و گندم به عنوان شایع ترین محرک های EoE شناخته می شوند. با این حال، آزمایشهای آلرژی معمولی اغلب در تشخیص حساسیت به غذاهای ایجادکننده EoE شکست میخورند که به این دلیل است که بیشتر واکنشهای آلرژی غذایی در EoE به تأخیر افتاده و عمدتاً توسط مکانیسمهای ایمنی غیر از حساسیت غذایی کلاسیک با واسطه IgE ایجاد میشود. در یک فرد مبتلا به EoE ممکن است یک یا چند غذا باعث تحریک EoE او شود. وقتی که غذا(های) مسبب شناسایی شده و از رژیم غذایی فرد حذف می شود، التهاب مری و علائم به طور کلی ظرف چند هفته بهبود می یابند. بنابراین، حذف غذا(های) مشکوک از رژیم غذایی و به دنبال آن کاهش علائم و التهاب مری برای اثبات اینکه غذا(ها) باعث ایجاد EoE می شوند، ضروری است.
ازوفاژیت ائوزینوفیلیک: تست پوستی خراشی (پریک)
افرادی که آلرژی دارند به یک ماده خاص در محیط یا رژیم غذایی خود واکنش نشان می دهند. هر ماده ای که بتواند واکنش آلرژیک ایجاد کند آلرژن نامیده می شود.
تست پوستی پریک شامل استفاده از سوزن پریک برای وارد کردن مقدار کمی آلرژن به پوست با ایجاد یک سوراخ کوچک است. اکثر عصاره های غذایی مورد استفاده در تست آلرژی توسط متخصص آلرژی از شرکت های تجاری که در ساخت آنها تخصص دارند خریداری می شود. گاهی اوقات، عصاره های غذایی برای تست خراش پوستی به صورت تازه در مطب آلرژیست از غذاهای تهیه شده توسط خانواده تهیه می شود.
تست پوست آلرژی اطلاعات خاصی را در مورد آنچه که هستید و به آن حساسیت ندارید به متخصص آلرژی ارائه می دهد. بیماران مبتلا به آلرژی یک آنتی بادی آلرژی به نام IgE می سازند. هنگامی که بیماران مبتلا به IgE برای یک آلرژن خاص، مقادیر کمی از آن آلرژن را در پوست خود قرار می دهند (تست پوستی خراشی)، ناحیه ای از تورم و قرمزی در عرض حدود 15 دقیقه در محلی که در آن تست پریک پوست انجام شده است، ایجاد می شود. با این حال، این آزمایشها در شناسایی غذاهای ایجادکننده EoE کاربرد محدودی دارند، زیرا EoE توسط آنتیبادیهای IgE ایجاد نمیشود.
ازوفاژیت ائوزینوفیلیک: آزمایش خون
گاهی اوقات یک متخصص آلرژی ممکن است یک آزمایش خون (به نام سنجش ایمنی اختصاصی سرم) انجام دهد تا ببیند آیا شما به یک آلرژن خاص حساس هستید یا خیر. این آزمایش گردش خون IgE را در جریان خون در برابر یک آلرژن شناسایی میکند و میتواند در شرایط خاص مرتبط با آلرژیهای غذایی با واسطه IgE مفید باشد. همانطور که قبلاً اشاره شد، هم برای تست پوستی پریک و هم برای آزمایش خون به منظور تشخیص حساسیت های ناشی از IgE در EoE در رابطه با شناسایی دقیق غذاهایی که باعث EoE می شوند، محدودیت هایی وجود دارد. متأسفانه، سنجشهای ایمنی اختصاصی سرم که آنتیبادیهای IgG را در تعداد زیادی از غذاها بررسی میکنند نیز در شناسایی غذاهایی که باعث EoE میشوند، مفید نیستند.
ازوفاژیت ائوزینوفیلیک: تست پچ مواد غذایی
حذف غذاها بر اساس نتایج آزمایشهای پوستی به تنهایی اغلب باعث بهبود EoE نمیشود. آزمایش پچ غذایی نوع دیگری از تست آلرژی است که قبلاً تصور می شد در شناسایی غذاهایی که باعث تحریک EoE در برخی بیماران می شود مفید باشد. تست پچ با قرار دادن مقدار کمی از یک غذای تازه در یک محفظه آلومینیومی کوچک به نام محفظه فین انجام می شود. سپس محفظه فین روی پشت فرد چسبانده می شود. غذای داخل محفظه به مدت 48 ساعت با پوست در تماس باقی می ماند. سپس برداشته می شود و متخصص آلرژی نتایج را در 72 ساعت می خواند. تصور می شد که مناطقی از پوست که با غذا در تماس بوده و ملتهب شده اند، احتمالاً واکنش تاخیری مثبت به غذا را شناسایی می کنند. آزمایش پچ دیگر برای استفاده روتین در ارزیابی EoE توصیه نمی شود. درک این نکته مهم است که تست های پوستی، آزمایش خون آلرژی و آزمایش پچ غذایی می توانند تست های مثبت کاذب داشته باشند. این به این معنی است که این آزمایشها ممکن است نشان دهند که شما نسبت به غذایی حساس هستید که میتوانید آن را تحمل کنید و باعث EoE شما نمیشود. آنها همچنین می توانند نتایج منفی کاذب داشته باشند، به این معنی که آزمایش برای غذایی که در واقع باعث EoE می شود، منفی است. رژیم های غذایی حذف، که در آن غذاهای مشکوک به ایجاد EoE از رژیم غذایی حذف می شوند، یک روش موثر برای درمان EoE هستند (به زیر مراجعه کنید). درصد کمی از افراد دچار آلرژی غذایی با واسطه IgE به غذایی می شوند که برای مدت طولانی از رژیم غذایی آنها حذف شده است تا ببینند آیا باعث ایجاد EoE آنها می شود یا خیر. این افراد با خوردن مجدد غذا می توانند بلافاصله واکنش آلرژیک داشته باشند. با استفاده از آزمایشهای پوستی خراشی و/یا آزمایشهای خون برای تشخیص حساسیت ناشی از IgE به غذاها، متخصص آلرژی میتواند به تعیین اینکه چه زمانی میتوان غذا را بهدنبال حذف EoE مجدداً به رژیم غذاییتان اضافه کرد، کمک میکند.
ازوفاژیت ائوزینوفیلیک: درمان
رژیمهای حذفی مبتنی بر آزمایش غذا
اگر بعد از تست پوستی خراشی، حساسیتهای غذایی خاصی دارید، پزشک ممکن است غذاهای خاصی را از رژیم غذایی شما حذف کند تا ببیند آیا کاهش علائم EoE وجود دارد یا خیر. در برخی افراد این به کنترل EoE آنها کمک می کند، اگرچه این نوع رژیم غذایی در مطالعات تحقیقاتی چندان موفق نبوده است.
رژیم های حذف تجربی
حذف آلرژن های غذایی اصلی از رژیم غذایی یک درمان قابل قبول برای EoE در نظر گرفته می شود. غذاهای حذف شده معمولاً شامل لبنیات، تخم مرغ، گندم، سویا، بادام زمینی/آجیل درختی و ماهی/ میگوهستند. نشان داده شده است که این رژیمها در درمان EoE بسیار مفید هستند، اگرچه پیروی از آنها به خصوص بدون کمک یک متخصص تغذیه با تجربه در مقابله با EoE میتواند بسیار دشوار باشد. غذاها معمولاً یک به یک با آندوسکوپی های بعدی اضافه می شوند تا به تعیین اینکه کدام غذاهای خاص باعث ایجاد EoE می شوند، کمک می کند.
رژیم های غذایی عنصری (elemental)
در این رژیم غذایی حذفی، تمام منابع آلرژن از رژیم غذایی حذف می شوند. بیمار تغذیه خود را از فرمول اسید آمینه به تنهایی یا گاهی اوقات در حالی که یک تا دو غذای ساده را بر اساس احتمال کم آنها برای تحریک EoE انتخاب و دریافت می کند. تمام مواد غذایی دیگر از رژیم غذایی حذف می شوند. ممکن است در کودکان بسیار خردسالی که تحت درمان با این رژیم هستند، لوله تغذیه مورد نیاز باشد، زیرا آنها اغلب قادر به نوشیدن کافی شیر خشک برای دریافت تغذیه کافی نیستند. این رویکرد عموماً برای کودکان مبتلا به آلرژی های غذایی متعدد که به سایر اشکال درمان پاسخ نداده اند، اختصاص دارد.
درمان دارویی
دوپیلوماب تنها درمان پزشکی تا به امروز است که توسط سازمان غذا و داروی آمریکا (FDA) برای درمان ازوفاژیت ائوزینوفیلیک تایید شده است. اخیراً در بیماران 12 ساله و بالاتر با وزن حداقل 40 کیلوگرم تأیید شده است. دوپیلومب یک داروی تزریقی به شکل آنتی بادی مونوکلونال (یا بیولوژیک) است که به صورت هفتگی تجویز می شود، التهاب مرتبط با بیماری را کاهش می دهد و توانایی بیماران را برای بلع غذا بهبود می بخشد.
سایر داروها نشان داده اند که تعداد ائوزینوفیل ها را در مری کاهش می دهند و علائم را بهبود می بخشند. مهارکنندههای پمپ پروتون (PPIs)، که تولید اسید در معده را کاهش میدهند، همچنین میتوانند التهاب مری را در برخی از بیماران مبتلا به EoE کاهش دهند. بنابراین، PPI ها اغلب به عنوان اولین درمان برای EoE استفاده می شوند. برخی از بیماران به خوبی به PPI ها پاسخ می دهند و در صورت انجام آندوسکوپی فوقانی با بیوپسی، کاهش زیادی در تعداد ائوزینوفیل ها و التهاب دارند. با این حال، همه بیماران به PPI ها پاسخ نمی دهند و سایر اشکال درمانی مانند کورتیکواستروئیدهای موضعی به شکل خوراکی یا رژیم های غذایی حذفی در نظر گرفته می شوند. نظارت دقیق توسط یک پزشک آگاه در درمان EoE بسیار مهم است.
کورتیکواستروئیدها که التهاب را کنترل می کنند، داروهای مفیدی برای درمان EoE هستند. بلع دوزهای کوچک کورتیکواستروئیدها به منظور تماس و درمان پوشش داخلی مری رایج ترین درمان است. اشکال مختلف کورتیکواستروئیدهای خوراکی در دسترس هستند. هنگامی که التهاب مری به اندازه کافی کنترل شد، دوز کورتیکواستروئید خوراکی به کمترین دوز لازم برای حفظ کنترل کاهش می یابد تا خطر عوارض جانبی استروئید کاهش یابد.
همکاری با پزشکان شما
EoE یک اختلال پیچیده است. برای بیماران مهم است که به متخصص گوارش خود برای مشاوره در مورد مدیریت EoE مراجعه کنند و بفهمند که چه زمانی آندوسکوپی برای بررسی بهتر یا بدتر شدن وضعیت لازم است. بیماران همچنین باید از نزدیک با فوق تخصص آلرژی و ایمونولوژی بالینی خود همکاری کنند تا دریابند که آیا آلرژی در آن نقش دارد یا خیر. یک فوق تخصص آلرژی همچنین میتواند تشخیص دهد که آیا نیاز به اجتناب از هر گونه غذا دارید و میتواند به شما در مدیریت مشکلات مرتبط مانند آسم، اگزما و رینیت آلرژیک کمک کند. مهم است که متخصص گوارش و آلرژیست شما با هم همکاری کنند و در مورد نحوه مراقبت از EoE شما به توافق برسند. اگر از رژیم غذایی برای درمان EoE خود پیروی می کنید، همکاری با یک متخصص تغذیه که در مورد رژیم های حذف مورد استفاده برای درمان EoE آگاهی دارد به شدت توصیه می شود.
دکتر بابک قلعه باغی
فوق تخصص آلرژی و ایمونولوژی بالینی

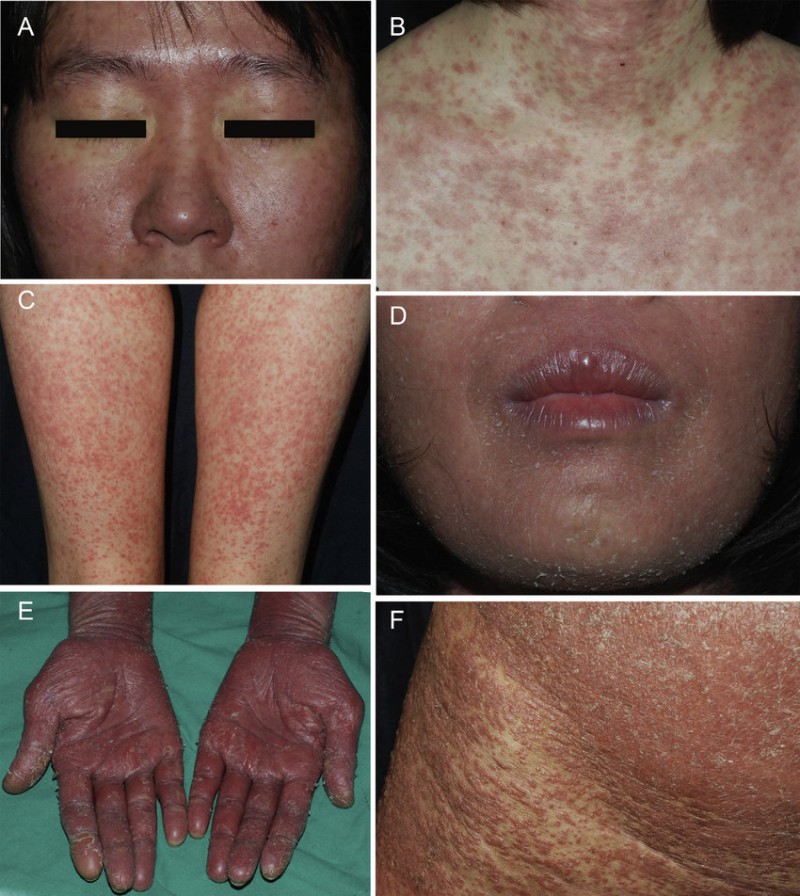
واکنش دارویی با ائوزینوفیلی و علائم سیستمیک (DRESS) نوعی حساسیت دارویی است که می تواند به عنوان واکنش به انواع زیادی از داروها رخ دهد.
تشخیص
بیماران مبتلا به DRESS می توانند طیف وسیعی از علائم را داشته باشند که می تواند شامل تب، بثورات پوستی، تورم صورت، بزرگ شدن غدد لنفاوی و آسیب کلیه یا کبد باشد. اکثر بیماران مبتلا به DRESS سطح غیرطبیعی سلول های خونی در آزمایش خون خود دارند که ائوزینوفیل نامیده می شود. ائوزینوفیل ها سلول هایی هستند که با بیماری های آلرژیک مرتبط هستند و وقتی به تعداد زیاد وجود داشته باشند می توانند باعث آسیب اندام شوند. بثورات میتواند به روشهای مختلف، معمولاً به صورت راش قرمز ظاهر شود، و میتواند در هر نقطه از پوست وجود داشته باشد، اما اغلب از صورت و قسمت بالایی بدن شروع میشود. اگرچه نادر است، اما سایر اندام ها نیز می توانند به دلیل DRESS ملتهب شوند.
داروهای عامل بیماری
اگرچه برخی از داروها بیشتر از سایرین با DRESS مرتبط هستند، تقریباً هر دارویی می تواند باعث DRESS شود. آنتی بیوتیک ها، آلوپورینول (داروی نقرس) و داروهایی که برای درمان تشنج استفاده می شوند، رایج ترین داروهایی هستند که در DRESS دخیل هستند. به طور کلی، علائم DRESS حدود دو تا شش هفته پس از شروع دارو توسط بیمار شروع می شود، بنابراین علائم فوری در DRESS دیده نمی شود. داروهایی که بیش از سه ماه مصرف شده اند بعید است که علت واکنش DRESS باشند.
درمان
مهم ترین مرحله در درمان DRESS، قطع داروی دخیل در واکنش است و گاهی اوقات، نیازی به درمان بیشتر نیست. برای درمان بثورات می توان استروئیدهای موضعی تجویز کرد. با این حال، اغلب برای محافظت از اندام ها در برابر آسیب، درمان بیشتری لازم است، مانند استروئیدها، که می توانند به صورت داخل وریدی یا خوراکی تجویز شوند. درمان با استروئیدها ممکن است برای هفتهها یا حتی ماهها مورد نیاز باشد و تست های آزمایشگاهی در این مدت به دقت کنترل میشوند. میانگین زمان بهبودی شش تا نه هفته است. در دراز مدت، اکثر بیماران خوب عمل می کنند، اگرچه برخی از بیماران ممکن است به بیماری های خودایمنی مبتلا شوند، بنابراین باید نظارت بیشتری در نظر گرفته شود.
دکتر بابک قلعه باغی
فوق تخصص آلرژی و ایمونولوژی بالینی

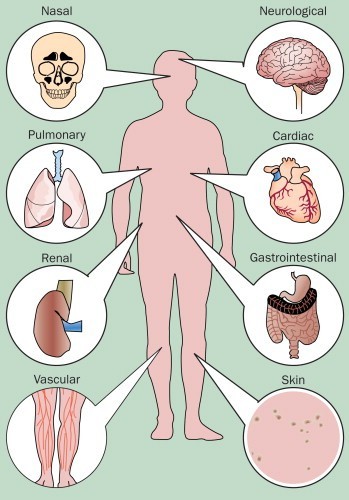
سندرم چرج اشتراوس
بررسی اجمالی
سندرم چرج استراوس (CSS) یا گرانولوماتوز ائوزینوفیلیک همراه با پلی آنژیت (EGPA) نوعی واسکولیت است. اینها اختلالاتی هستند که با التهاب رگ های خونی مشخص می شوند. این التهاب اغلب روی ریه ها، پوست، اعصاب و معده تاثیر می گذارد. آسم شایع ترین علامت CSS/EGPA است. علائم همچنین ممکن است شامل سایر مشکلات ریوی، رینیت آلرژیک (تب یونجه)، بثورات پوستی، درد معده و بی حسی در دست ها و پاها باشد.
علائم و تشخیص
CSS/EGPA می تواند منجر به علائم مختلفی شود، از خفیف تا بسیار شدید و تهدید کننده زندگی. علائم اغلب به صورت مرحلهای بروز میکنند، اگرچه این مراحل در همه افراد به یک ترتیب دیده نمی شوند. اگر زود تشخیص داده شود، می توان از مراحل بعدی از طریق درمان جلوگیری کرد.
اولین مرحله، مرحله آلرژیک است. علائم رایج در این مرحله عبارتند از:
مرحله بعدی هایپرائوزینوفیلی است، به این معنی که سطح خاصی از گلبول های سفید خون، ائوزینوفیل، به طور غیرعادی بالا در جریان خون وجود دارد. هایپرئوزینوفیلی می تواند منجر به موارد زیر شود:
مرحله سوم مرحله واسکولیت سیستمیک است که با التهاب شدید عروق خونی در قسمتهای مختلف بدن مشخص میشود، از جمله:
بسیاری از علائم احتمالی عبارتند از:
تشخیص CSS/EGPA بر اساس سابقه بیمار علاوه بر آزمایشهای غیرطبیعی خون و عکسبرداری قفسه سینه یا سیتی اسکن است. ممکن است نیاز به بیوپسی از اندام آسیب دیده باشد.
درمان
CSS/EGPA یک بیماری جدی است که بدون درمان می تواند کشنده باشد. با این حال، با درمان، اغلب می توان CSS/EGPA را کنترل کرد و بهبودی کامل ممکن است. درمان معمولاً شامل استروئیدها یا سایر داروهای سرکوب کننده سیستم ایمنی است. برخی از داروهای جدیدتر به نام بیولوژیک نیز برای درمان این اختلال استفاده شده است.
دکتر بابک قلعه باغی
فوق تخصص آلرژی و ایمونولوژی بالینی
